

01
注册证
02
注册声明
一、
俄罗斯器械分类
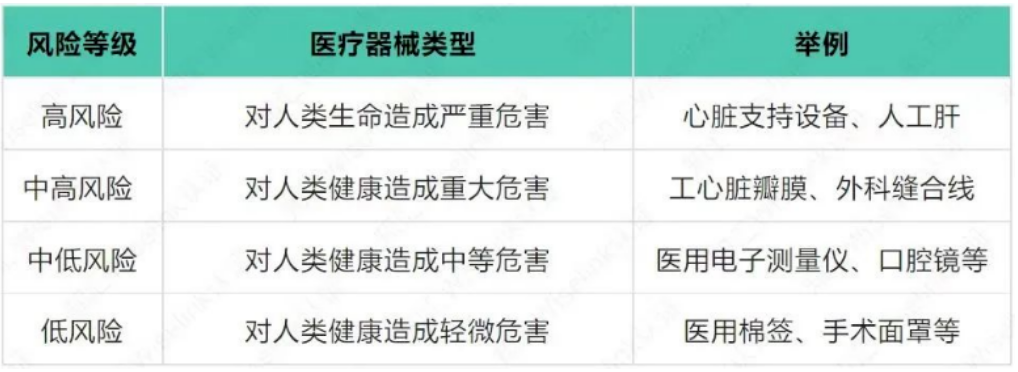
ClassI低风险
a.输送,贮存或注射血液,体液者除外之非侵入性装置
b.与受伤皮肤接触之非侵入性装置,用于止住渗出物
c.不超过60分钟之暂时性使用侵入性装置
d.不超过30分钟之短期使用于口腔至咽喉,耳管至耳膜之侵入性装置
e.可再使用之外科用具
f.长期植入齿内之侵入性装置
g.不属于第II类之主动式装置非灭菌类医疗器械,例如: 检验手套、检诊乳胶手套、绷带、手术台、手术灯、义肢、轮椅、电动代步车、冷热敷袋、医疗具?等等。需灭菌类疗器械,例如: 外科用灭菌手套、刀具、绷带等等。
Class IIa 低到中风险
Class IIb 中风险
a.用于改变血液,其它体液或注射液之非侵入性装置
b.用于后续治疗撕裂之表皮伤口之非侵入性装置
c.以电离辐射供给能源或产生生物效应之长期使用侵入性装置
d.除了第I(f)及III类之长期侵入性装置,且有危险性之主动式装置(如电雕辐射)
e.控制生育或防止性病传染用之装置
f.所有用于消毒,清洁,洗涤隐形眼镜用之装置
g.血袋 例如:血液透析器、血氧浓度计、电刀装置、X光机、超音波喷雾呼吸治疗器、生理监视器、骨钉、骨板、人工关节、保险套、血袋等
class III高风险
a.与心脏或中央循环、神经系统直接接触用以诊断、监测用之暂时性、短期及长期侵入性装置
b.在体内产生生物效应,经过化学变化或控制药物之侵入性装置
c.含有符合65/65/EEC指令规定医疗物质且该物质可能对人体产生作用以辅助医疗作用的所有装置
d.长期植入式医疗装置
e.与受伤皮肤接触,使用非活的动物组织或其源出物所制造之装置 例如:可吸收式手术缝合线、关节注射液、脑部引流系统等等
二、
认证时间
三、
俄罗斯医械注册证程序和要求资料:
1、准备申请需要的以下文件
2.将以上申请需要的文件递交给做认证的公司确认是否合格。
3.以上申请需要的文件确认合格以后,将所有文件找人翻译成俄文
4.将以下所有文件的原文件递交给中国贸促会以及俄罗斯驻中国大使馆进行公证(接下)
四、
中国贸促会及俄罗斯使馆公证资料
5.申请所需文件翻译好后,递交给做知汇Wiselink,同时并签订合同,支付预付款(详细以实际沟通为准)
6.邮寄样品到俄罗斯进行测试
7.临床试验完成以后 (大约2个月)
8.认证公司提供注册证书正本扫描件以后(大约8-10个月),支付尾款给认证公司,俄罗斯寄注册证原件给知汇。
六、
认证注册的难点
Wiselink-全球布局
知汇供应链服务(深圳)有限公司 WiselinkSupply Chain Services (Shenzhen) Ltd,简称Wiselink CN隶属于澳大利亚Wiselink集团,是深圳大兴集团的官方合作企业,拥有包括原澳大利亚药品监督管理局局长Dr.Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、客观、真诚的核心价值观,致力于为体外诊断(IVD)、医疗器械(MD)、保健品和化妆品制造商提供海外临床试验和全球合规认证服务。
集团总部
Wiselink Group
Level 25,100 Mount Street, North Sydney, NSW Australia 2060
爱尔兰分公司
Wiselink Medical (lreland) Limited
Unit 1/4/7Block 1 Northwood Court, Northwood Crescent,Dublin 9. D09 E438, lreland
官网:http://www.wiselinkie.com/
泰国分公司
Wiselink Medical (Thailand) Company Limited
No. 1 Vasu Building 1, Room No. P01, 1st Floor, Soi Sukhumvit 25, Sukhumvit Road, Klongtoey Nuea Subdistrict, Wattana District Bangkok 10110, Thailand
日本分公司
株式会社Wiselink Japan
地址:東京都千代田区神田須田町一丁目2番地7淡路町駅前ビル3階
中国分公司
知汇Wiselink
地址:深圳市宝安区新安街道创业二路二栋301
官网:Http://www.wiselinkchina.com