

医疗器械、IVD临床试验
一、定义及临床试验目的
临床试验的定义:任何涉及⼀个或多个⼈类受试者的系统调查,以评估设备的安全性或性能。
• 医疗器械临床调查通常出于监管要求进⾏
• 进⾏临床调查的目的应在规划过程开始时商定,因为它将对研究的设计和需要⽣成的临床数据产⽣直接影响。
二、临床试验和医疗产品生命周期的关系
• 设计 - 验证 - 确认 - ⽣产 - 销售 - 售后
• 根据质量管理体系 ISO13485
• 设计验证应针对代表性产品进⾏
• 代表性产品包括初始⽣产单元、批次或同等产品
• 作为设计和开发验证的⼀部分,组织应根据适⽤的法规要求对医疗器械进⾏临床评估或性能评估
• ⽤于临床评估或性能评估的医疗器械不被视为发布给客户使⽤
临床试验可分三个阶段:策划 — 执行 — 结束
三、临床试验策划
1、策划考虑因素
• 医疗器械法规
• 体外诊断医疗器械法规 (EU) 2017/746 (EU IVDR)
• 医疗器械法规 (EU) 2017/745 (EU MDR)
2、质量管理体系要求
• 法规要求(国际 - MDSAP、区域 - MDR、国家 - 美国 FDA、加拿⼤- HC 等)
3、指导⽂件
• ISO 14155-2020 ⼈类受试者医疗器械的临床研究—良好的临床试验规范
• MEDDEV 2.7/4 关于临床研究的必要性和⼀般原则
• MEDDEV 2.7/2 Rev 2 关于临床调查验证和主管当局评估
• MDCG 2021-20 为 MDR 临床研究⽣成 CIV-ID 的说明
• MDCG 2021-08 临床研究申请/通知⽂件
• ISO 20916:2019 - 体外诊断医疗器械 - 使用⼈体样本的临床性能研究 - 良好的研究实践
• MDCG 2021-2 - COVID-19 快速抗体检测最新技术指南
4、人员配备
5、编写临床调查档案
6、选址
7、建立试验终止程序
四、临床试验执行
1、临床试验作业程序标准
2、相关部门审批
3、监测
IVD临床试验服务
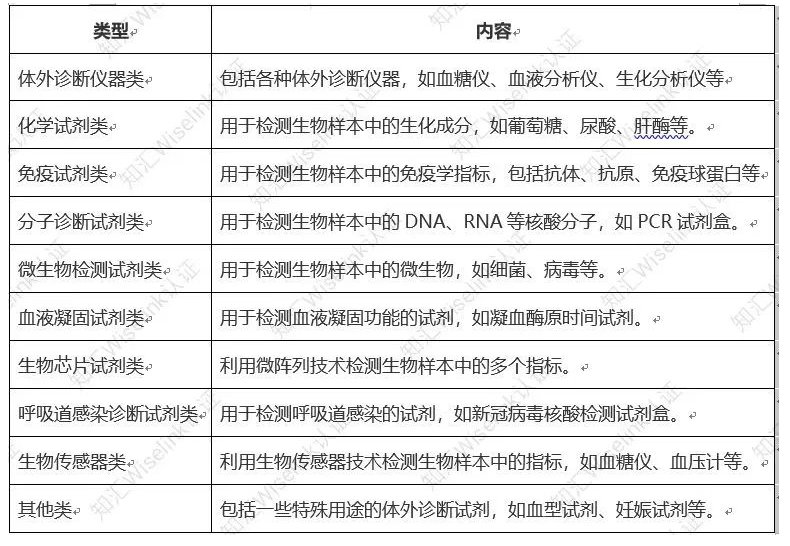
一、什么是IVD体外诊断试剂?
IVD体外诊断试剂注册是指将IVD体外诊断试剂产品提交给相关的监管机构(如FDA、CE、CFDA等),并经过审核、评估、认证后获得许可证书,允许在市场上销售和使用的过程。这个过程需要遵循相关的法律法规和规范要求,包括ISO 13485质量管理体系、ISO 14971风险管理体系、GMP(Good Manufacturing Practice)等。
IVD体外诊断试剂注册的过程包括申请、审核、评估、许可证颁发等环节。申请人需要提供产品相关的资料和证明文件,包括产品技术规格、安全性评估、临床试验数据、质量保证计划等。监管机构会对这些文件进行审核和评估,评估结果可能包括通过、需要补充材料、拒绝等。如果被批准,申请人可以获得许可证书,获得销售和使用的权利。
二、诊断试剂临床试验注册的详细步骤和流程:
1 | 确定试验方案和研究设计。在设计试验方案和研究设计时,需要考虑试验的目的、研究对象、样本大小、研究方法、数据分析等方面的问题,并确保试验方案符合伦理和法律要求。 |
2 | 选择合适的注册平台。国际上已经建立了多个体外诊断试剂临床试验注册平台,如ClinicalTrials.gov、EU Clinical Trials Register等。选择合适的平台需要考虑平台的可靠性、注册流程和费用等方面的问题。 |
3 | 注册试验并提交相关信息。在注册试验时,需要提交试验方案、研究设计、研究目的、试验结果等信息,并确保信息的准确性和完整性。注册后,试验方案将被公开,并可以在注册平台上进行搜索和查看。 |
4 | 获得伦理委员会的批准。在进行体外诊断试剂临床试验前,需要获得伦理委员会的批准。伦理委员会需要审查试验方案和研究设计,以确保试验符合伦理要求和法律要求。 |
5 | 开始试验。在试验进行过程中,需要遵循试验方案和研究设计,收集、分析和报告试验数据。 |
6 | 更新注册信息。在试验进行过程中,如果试验方案或研究设计发生了变化,需要及时更新注册信息,并向注册机构提交更新后的信息。 |
7 | 完成试验并提交评价信息。完成试验后,需要对试验结果进行评价和分析,并将结果提交给相关机构进行审查和批准。这些机构可以是监管机构、学术机构、医疗机构等,其主要任务是确保试验结果的科学性和可信度,以保障公众健康和安全。 |
三、IVD体外诊断试剂注册资料:
产品注册申请表:
申请表需要填写产品的基本信息,包括产品名称、型号、用途、适用人群等。
产品说明书:
产品说明书需要详细描述产品的性能、使用方法、注意事项等。
产品标签和包装:
产品标签和包装需要符合当地的标准,包括标签上的文字、图案、条形码等。
产品检测报告:
需要提供产品的检测报告,包括产品的性能指标、安全性、有效性等。
生产厂家的质量管理体系证明:
生产厂家需要提供质量管理体系证明,如ISO 13485认证证书等。
生产厂家的营业执照和生产许可证:
需要提供生产厂家的营业执照和生产许可证等相关证明文件。
产品销售许可证:
有些国家和地区要求产品销售前需要获得当地的销售许可证,需要提供相应证明文件。
其他相关证明文件:
根据当地的规定,可能需要提供其他相关证明文件,如CE认证证书、FDA注册证书等。
总之,做国际体外诊断试剂临床试验注册需要注意注册平台的选择、注册信息的准确性和完整性,以及及时更新注册信息和提交评价信息等方面的问题。同时也需要注意遵守伦理和法律要求,确保试验的科学性和可信度。