知汇Wiselink有泰国本地分公司,泰国是东南亚主要的医疗器械市场之一。在泰国,医疗器械受公共卫生部下属的泰国食品和药物管理局(Thai FDA)监管,以确保医疗器械的安全性、有效性和合规性。在医疗器械产品合法引入泰国市场之前,需要在Thai FDA进行注册。
当地的主要法规为Medical Device Act B.E. 2551 (2008)和Medical Device Act (2nd Edition) B.E. 2562 (2019) 等。另外作为东盟ASEAN成员国,泰国也会参考东盟相关法规。
境外制造商首先需要在泰国指定授权当地代理人。注册证有效期为5年,会颁发给该当地代理。目前泰国法规规定不可变更代理人,但同一产品可以同时有多个当地代理人。
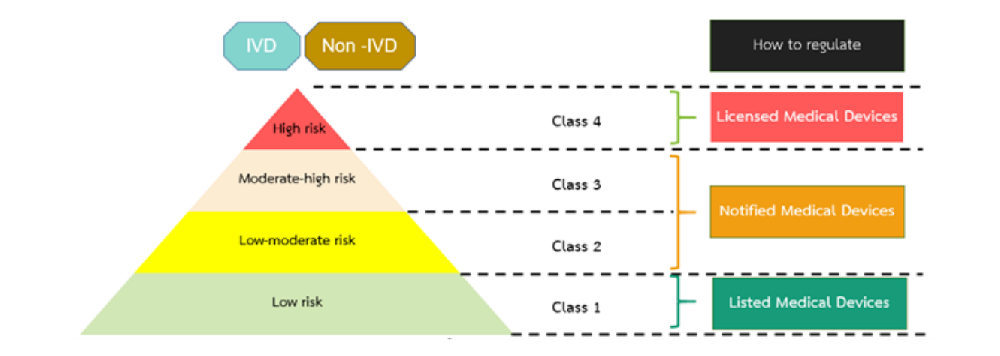
医疗器械(包括IVD)产品的风险分类主要取决于器械的性质和预期用途。在泰国,医疗器械风险等级由低风险向高风险依次分为Class 1, Class 2, Class 3和Class 4四类。
根据风险等级不同,Thai FDA的监管力度也会不同。最低风险的1类产品只需要列名(listing),风险较高的2类和3类产品需要进行通知(Notification),而风险最高的4类产品则需要批准许可(License)。
在泰国主要有三种注册路径:
“简洁路径”(Concise pathway)适用于在参考国家(欧盟、加拿大、日本、澳大利亚、美国或WHO Prequalification)注册过的产品,该产品需要在至少一个参考国家成功注册并上市1年以上,且无严重不良事件。
类似的“信赖计划”(Reliance program)则适用于已在新加坡HSA成功注册的医疗器械产品。
如产品不满足以上两个情况的话,则需要走全流程审批路径(Full evaluation)
所有风险等级的产品技术文件均需参考东盟通用提交档案模板CSDT(Common Submission Dossier Template) 。另外对于2、3、4类产品,需要ISO 13485质量管理体系。
根据不同产品风险等级以及产品的具体情况,泰国注册的时间可能需要0-300天。费用也会从几十美元到4000美元不等。
Wiselink-全球布局 知汇供应链服务(深圳)有限公司 WiselinkSupply Chain Services (Shenzhen) Ltd,简称Wiselink CN隶属于澳大利亚Wiselink集团,是深圳大兴集团的官方合作企业,拥有包括原澳大利亚药品监督管理局局长Dr.Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、客观、真诚的核心价值观,致力于为体外诊断(IVD)、医疗器械(MD)、保健品和化妆品制造商提供海外临床试验和全球合规认证服务。 集团总部 Wiselink Group Level 25100 Mount Street, North Sydney, NSW Australia 2060 爱尔兰分公司 Wiselink Medical (lreland) Limited Unit 1/4/7Block 1 Northwood Court, Northwood Crescent,Dublin 9. D09 E438, lreland 官网:http://www.wiselinkie.com/ 泰国分公司 Wiselink Medical (Thailand) Company Limited No. 1 Vasu Building 1, Room No. P01, 1st Floor, Soi Sukhumvit 25, Sukhumvit Road, Klongtoey Nuea Subdistrict, Wattana District Bangkok 10110, Thailand 中国分公司 地址:深圳市宝安区新安街道创业二路二栋301 官网:Http://www.wiselinkchina.com
知汇Wiselink
日本分公司
株式会社Wiselink Japan
地址:東京都千代田区神田須田町一丁目2番地7淡路町駅前ビル3階